|
||||
|
|
38. Углерод и его свойства Углерод (С) – типичный неметалл; в периодической системе находится в 2-м периоде IV группе, главной подгруппе. Порядковый номер 6, Ar = 12,011 а.е.м., заряд ядра +6. Физические свойства: углерод образует множество аллотропных модификаций: алмаз – одно из самых твердых веществ, графит, уголь, сажа. Химические свойства: электронная конфигурация: 1s22s22p2. На электронной оболочке атома – 6 электронов; на внешнем валентном уровне – 4 электрона. Наиболее характерные степени окисления: +4, +2 – в неорганических соединениях, – 4, -2 – в органических. Углерод в любом гибридном состоянии способен использовать все свои валентные электроны и орбитали. У 4-валентного углерода нет неподеленных электронных пар и нет свободных орбиталей – углерод химически относительно устойчив. Характерно несколько типов гибридизации: sp, sp2, sp3. При низких температурах углерод инертен, но при нагревании его активность возрастает. Углерод – хороший восстановитель, но соединяясь с металлами и образуя карбиды, он выступает окислителем:  Углерод (кокс) вступает в реакции с оксидами металлов: 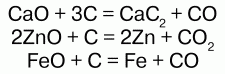 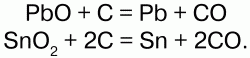 Таким образом выплавляют металл из руды. При очень высоких температурах углерод реагирует со многими неметаллами. Огромное количество органических соединений он образует с водородом – углеводороды. В присутствии никеля (Ni) углерод, реагируя с водородом, образует предельный углеводород – метан: С + Н2 = СН4. При взаимодействии с серой образует сероуглерод: С + 2S2 = СS2. При температуре электрической дуги углерод соединяется с азотом, образуя ядовитый газ дициан: 2С + N2 = С2N2?. В соединении с водородом дициан образует синильную кислоту – НСN. С галогенами углерод реагирует в зависимости от их химической активности, образуя галогениды. На холоде реагирует со фтором: С + 2F2 = СF2. При 2000 °C в электропечи углерод соединяется с кремнием, образуя карборунд: Si + C = SiC. Нахождение в природе: свободный углерод встречается в виде алмаза и графита. В виде соединений углерод находится в составе минералов: мела, мрамора, известняка – СаСО3, доломита – MgCO3?CaCO3; гидрокарбонатов – Mg(НCO3)2 и Са(НCO3)2, СО2 входит в состав воздуха; углерод является главной составной частью природных органических соединений – газа, нефти, каменного угля, торфа, входит в состав органических веществ, белков, жиров, углеводов, аминокислот, входящих в состав живых организмов. |
|
||
|
Главная | В избранное | Наш E-MAIL | Прислать материал | Нашёл ошибку | Наверх |
||||
|
|
||||
